中央研究院化學研究所-學術研究
研究方向
化學所配合優質生活與永續社會願景,因應國際上基礎化學與永續材料、永續能源、永續生命等研究領域及「綠能科技」、「生技醫療」等創新研發計畫,擬定達成研究創新、學術卓越、永續發展的目標,將材料化學、合成化學、觸媒化學、化學生物學等領域列為重點研究方向,進行創新性研發。除了基礎科學研究,同仁也著力於將研究成果進行專利佈局及技術轉移。藉由執行國家型計劃,化學所亦致力於運用創新科技對台灣社會面臨的環境、能源、健康議題提供前瞻技術。
一、材料化學研究
有機光電材料的應用與奈米材料的設計開發是化學所材料化學的重點研究方向,多個相關次領域的研究成果在國際上佔有重要的學術地位。主要研發成果包括應用在有機發光二極體的高效能藍色螢光有機材料、結合金奈米粒子與五環素所構成有機場效電晶體、首次製作出穩定的六環素單晶材料所構成的有機薄膜電晶體、成功設計製備出罕見巨型單壁金屬有機管狀奈米材料、將金屬有機結構的應用推展至光電材料及半導體材料,以及開發多種高效能材料應用於染料敏化、鈣鈦礦和有機光伏電池。另外,智慧應答分子、核殼奈米材料及生物材料也是研發的重點。最近重要成果報導之一為:藉由仿生結構設計,開發了適合生物機電介面電極的新穎導電高分子,用其組成奈米薄膜可獲得奈米生物電子界面,在此界面上利用電刺激的方式,可讓神經突觸有前所未見的增生效果。
二、化學合成方法開發及新穎催化反應
近年來,隨著能源催化及綠色合成化學技術需求,本所合成化學及觸媒化學研究也整合成為跨領域的研究團隊推動尖端合成及催化反應的技術發展及應用。目前,合成化學領域重點為合成方法開發及藥物合成,觸媒化學則以替代能源相關催化反應為主軸。本所近年在化學催化及合成領域代表性研究成果包括:(1) 合成方法學:鋰化矽醚建構苯環上鄰位羥基之酮類化合物,微波輔助一鍋化合成脫水醣及具位置選擇性保護基的硫苷醣,合成智慧型螢光探針應用於生物正交醣類標定 ; (2) 配位化學:新穎氮異環碳烯的合成及超高活性的金屬錯合物催化反應,新穎紫質錯合物應用於小分子活化,生物工程改變細胞色素及烷基羥基化酵素用以研究烷類至醇類轉換 ; (3) 替代能源催化:高效率氫氣製備及反應機構研究, 孔洞材料嵌入三銅錯合物進行甲烷至甲醇活化,木質纖維素分解及高值化。除了基礎科學研究外,本領域同仁也積極將研究成果申請專利技術並有兩項技術分別技轉至國內化工廠及新藥開發廠商。
三、化學生物學 : 從前瞻材料與方法創新展望健康永續策略
從生化巨分子的結構層次解析生物體內細胞功能與其作用機制,進而瞭解這些複雜的機制在重要疾病中扮演的角色,衍生出可能的藥物與檢測/治療方法,是化學所在化學生物學發展的重點。目前本所化學生物學領域研究主題涵蓋 (1) 開發新穎生物材料及應用,(2) 發展化學探針與尖端影像技術及結構生物學技術,(3) 癌症、感染性疾病、神經退化疾病的致病機制及治療藥物開發,(4) 開發蛋白質體方法探索疾病標記。本所在這些研究領域近年來的研究成果包括發展以質譜儀技術為基礎之新穎膜蛋白體及磷酸化蛋白質體定量技術,闡釋疾病機制及應用於生物標記開發以熱響應性奈米魔鬼氈作為關鍵元件,研發循環腫瘤細胞萃取系統,有效便捷地從血液樣品中萃取癌細胞及進行基因檢測。本所同仁也將觸角伸入神經退化性疾病「蛋白質的異常摺疊」在的相關研究,首度發現漸凍人中 TDP-43 蛋白的 C 端胜肽片段所產生的類澱粉狀纖維,並建構出可以在活體細胞中誘發 TDP-43 蛋白異常聚集的光控探針。在研究巨分子結構和基因轉錄的機制方面,不但成功地應用螢光共振能轉移效率, 定位出核醣核酸聚合酶上的核醣核酸出口通道,更以冷凍電子顯微鏡解析 Gdown1 蛋白質透過新型立體干擾促進對調控哺乳類的轉譯作用之了解。本所同仁亦成功建立以紅外線活化的激酶-上轉換粒子平台以控制細胞內信號傳遞。
醣啟動了調控活化B細胞存亡之樞紐
Temporal regulation of Lsp1 O-GlcNAcylation and phosphorylation during apoptosis of activated B cells
Nat Commun. 2016, 7, 12526.
Wu JL, Wu HY, Tsai DY, Chiang MF, Chen YJ, Gao S, Lin CC, Lin CH, Khoo KH, Chen YJ, Lin KI
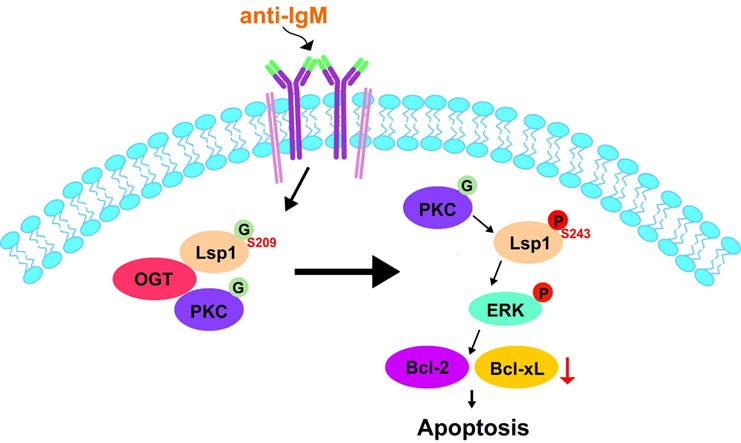
O連結乙醯葡萄氨糖修飾是細胞中的一種後轉錄調控修飾作用,在細胞中此種修飾是經由OGT酵素在蛋白質的絲氨酸和蘇氨酸進行催化完成,另一個酵素OGA則負責將此修飾移除。由於此種修飾是發生在絲氨酸和蘇氨酸上,其在細胞中所參與的許多作用被認為是藉由影響磷酸化修飾來達成。磷酸化蛋白質體和O 連結乙醯葡萄氨糖修飾之同時分析,我們發現高達313個磷酸化點位受到乙醯葡萄氨糖之影響, 其中,Lsp1 蛋白會被 O 連結乙醯葡萄氨糖修飾在絲氨酸 209 位點上。並進而啟動絲氨酸 243 位點的磷酸化透過 Lsp1 蛋白不同的後轉譯修飾突變進行功能性分析時,我們觀察到 Lsp1 蛋白的 O 連結乙醯葡萄氨糖修飾和絲氨酸 243 位點的磷酸化會調控B 細胞的細胞凋亡作用之重要機制,實驗結果發現Lsp1 蛋白的 O 連結乙醯葡萄氨糖修飾是藉由增加 Lsp1 蛋白和負責絲氨酸 243 位點的磷酸化之激酶,PKC-β1 的接合量來達成促進下游和細胞凋亡相關的訊息傳遞體之活化,及降低BCL-2 和 BCL-xL 的表現來達成促進細胞凋亡的作用。綜合上述,我們的實驗結果闡述了蛋白 O 連結乙醯葡萄氨糖修飾和磷酸化修飾之間的動態交互作用決定了 B 細胞受受體接合而活化後的細胞凋亡命運。
Crosslinking of B-cell receptor (BCR) sets off an apoptosis programme, but the underlying pathways remain obscure. Here we decipher the molecular mechanisms bridging B-cell activation and apoptosis mediated by post-translational modification (PTM). We find that O-GlcNAcase inhibition enhances B-cell activation and apoptosis induced by BCR crosslinking. This proteome-scale analysis of the functional interplay between protein O-GlcNAcylation and phosphorylation in stimulated mouse primary B cells identifies 313 O-GlcNAcylation-dependent phosphosites on 224 phosphoproteins. Among these phosphoproteins, temporal regulation of the O-GlcNAcylation and phosphorylation of lymphocyte-specific protein-1 (Lsp1) is a key switch that triggers apoptosis in activated B cells. O-GlcNAcylation at S209 of Lsp1 is a prerequisite for the recruitment of its kinase, PKC-β1, to induce S243 phosphorylation, leading to ERK activation and downregulation of BCL-2 and BCL-xL. Thus, we demonstrate the critical PTM interplay of Lsp1 that transmits signals for initiating apoptosis after BCR ligation.